Предмет: Математика,
автор: Alphaomegatdb
[Последние баллы!] Помогите!
Решите задания на картинках!
Приложения:
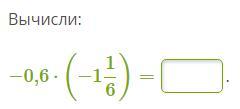
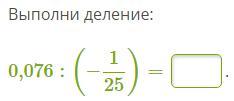

Ответы
Автор ответа:
0
Ответ:
Пошаговое объяснение:
Приложения:

Похожие вопросы
Предмет: Алгебра,
автор: Oklk
Предмет: Обществознание,
автор: Аноним
Предмет: Литература,
автор: veronikaponomarenko
Предмет: Алгебра,
автор: noyabrsk20
Предмет: Химия,
автор: Mparsonok