Предмет: Химия,
автор: asedft
Рассчитайте массу осадка полученного при взаимодействии 200г раствора нитрата серебра с массовой долей 17% с металлической медью
Ответы
Автор ответа:
0
вначале записываем уравнение реакции:
2AgNO3 + Cu = Cu(NO3)2 + 2Ag(осадок)
нам известна масса раствора и его концентрация, значит мы можем найти массу нитрата серебра:
m(AgNO3) = 200 * 0.17 = 34г (для вычислений проценты переводим в доли единицы 17% = 0.17)
Затем находим молярные массы интересующих нас веществ.
составляем пропорцию, читается так: 340 грамм нитрата серебра относится к 216 грамм серебра, как 34 грамм нитрата серебра относится к x грамм серебра.
решаем пропорцию по всем правилам математики и получаем ответ
2AgNO3 + Cu = Cu(NO3)2 + 2Ag(осадок)
нам известна масса раствора и его концентрация, значит мы можем найти массу нитрата серебра:
m(AgNO3) = 200 * 0.17 = 34г (для вычислений проценты переводим в доли единицы 17% = 0.17)
Затем находим молярные массы интересующих нас веществ.
составляем пропорцию, читается так: 340 грамм нитрата серебра относится к 216 грамм серебра, как 34 грамм нитрата серебра относится к x грамм серебра.
решаем пропорцию по всем правилам математики и получаем ответ
Приложения:
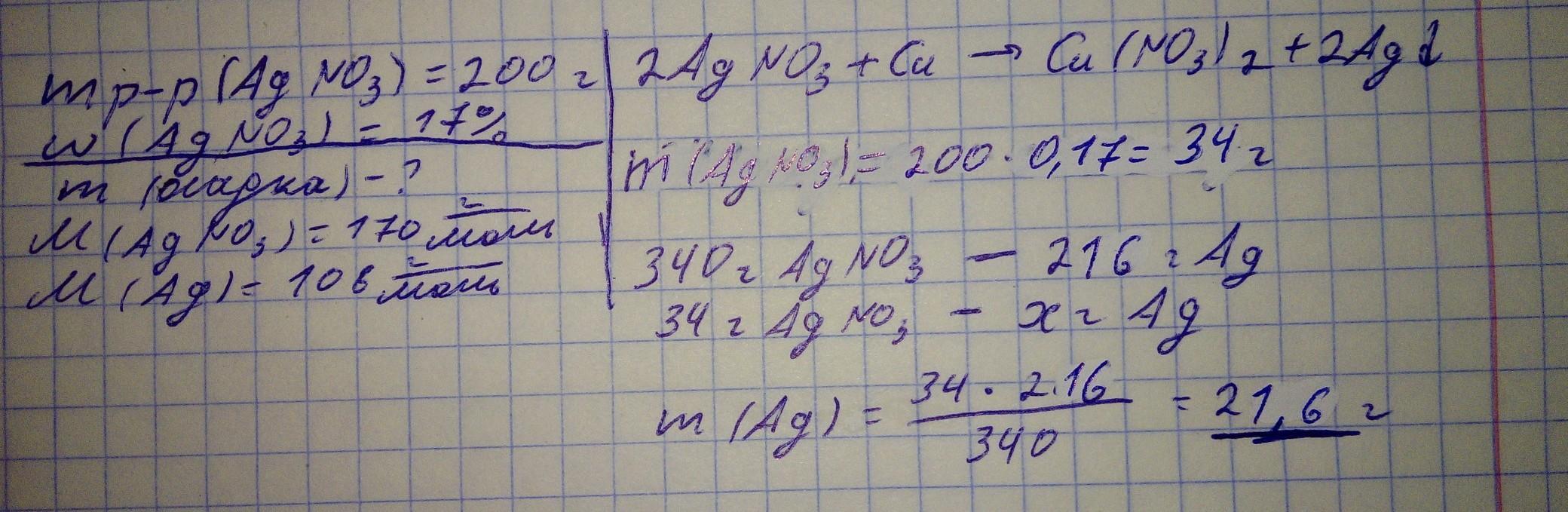
Аноним:
откуда было взято 208?
извиняюсь, ошибки случаются
208 было взято из-за моей невнимательности
Похожие вопросы
Предмет: Математика,
автор: Yana11117
Предмет: Қазақ тiлi,
автор: Аноним
Предмет: Биология,
автор: Аноним
Предмет: Литература,
автор: adilbenrlitom
Предмет: Информатика,
автор: hardonsky