Предмет: Химия,
автор: stasankaslev
Какой объем водорода (н.у) выделится при взаимодействие 9.8 г серной кислоты с цинком .
Ответы
Автор ответа:
0
дано
m(H2SO4) = 9.8 g
-----------------------------
V(H2)-?
Zn+H2SO4-->ZnSO4+H2
M(H2SO4) = 98 g/mol
n(H2SO4) = m/M = 9.8 / 98 = 0.1 mol
n(H2SO4) = n(H2) = 0.1 mol
V(H2) = n*Vm = 0.1 * 22.4 = 2.24 L
ответ 2.24 л
m(H2SO4) = 9.8 g
-----------------------------
V(H2)-?
Zn+H2SO4-->ZnSO4+H2
M(H2SO4) = 98 g/mol
n(H2SO4) = m/M = 9.8 / 98 = 0.1 mol
n(H2SO4) = n(H2) = 0.1 mol
V(H2) = n*Vm = 0.1 * 22.4 = 2.24 L
ответ 2.24 л
Автор ответа:
0
Во вложении.............
Приложения:
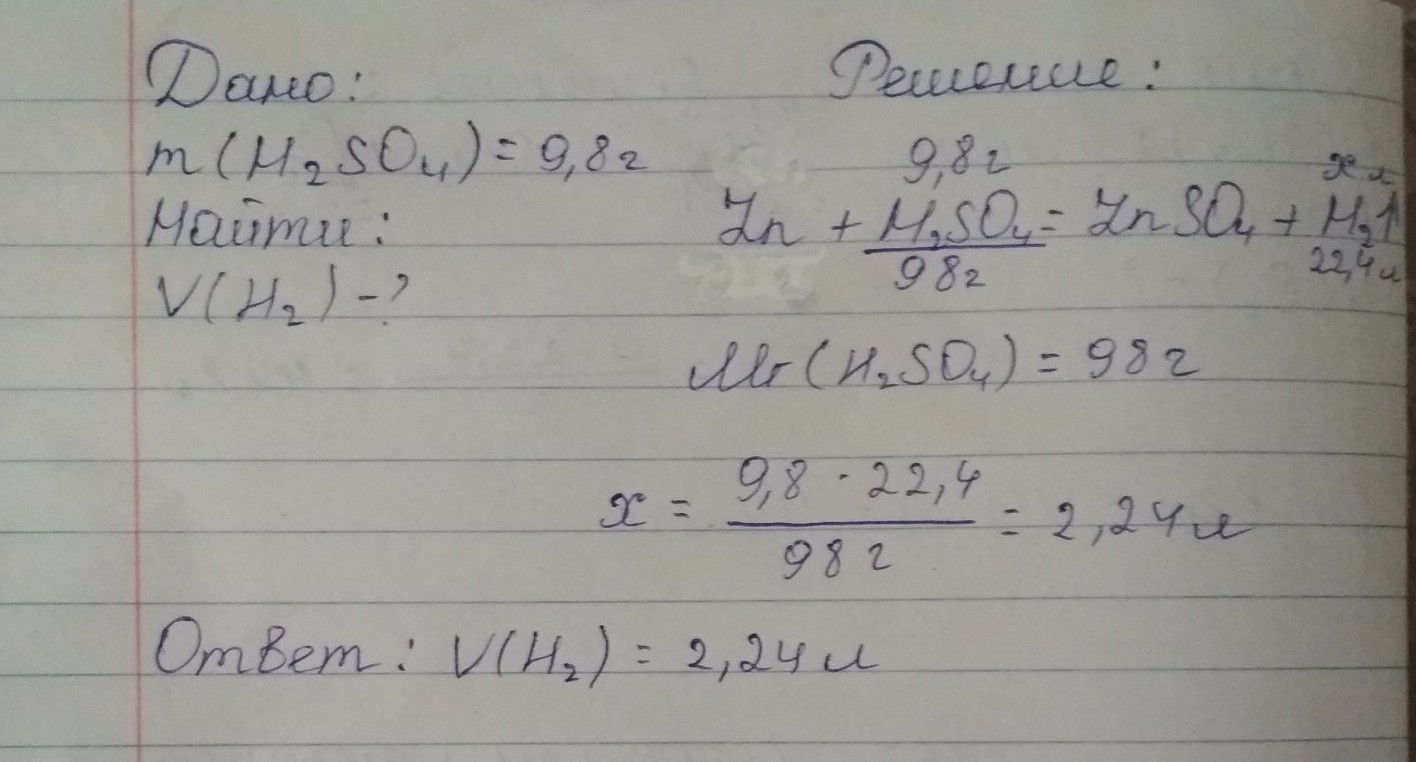
Похожие вопросы
Предмет: Математика,
автор: cuprunovatatana07
Предмет: Физика,
автор: adtyxxcyy
Предмет: Английский язык,
автор: rasulmakhsudov20073
Предмет: Математика,
автор: KristinaKor2005
Предмет: Математика,
автор: aidariya0303