Предмет: Химия,
автор: Turpal15
Объясните пожалуйста подробнее, как решать 20 задание ОГЭ по химии?)
P.S. Я никак не могу решить это задание, ничего не понимаю!
Даю 15 баллов
Приложения:
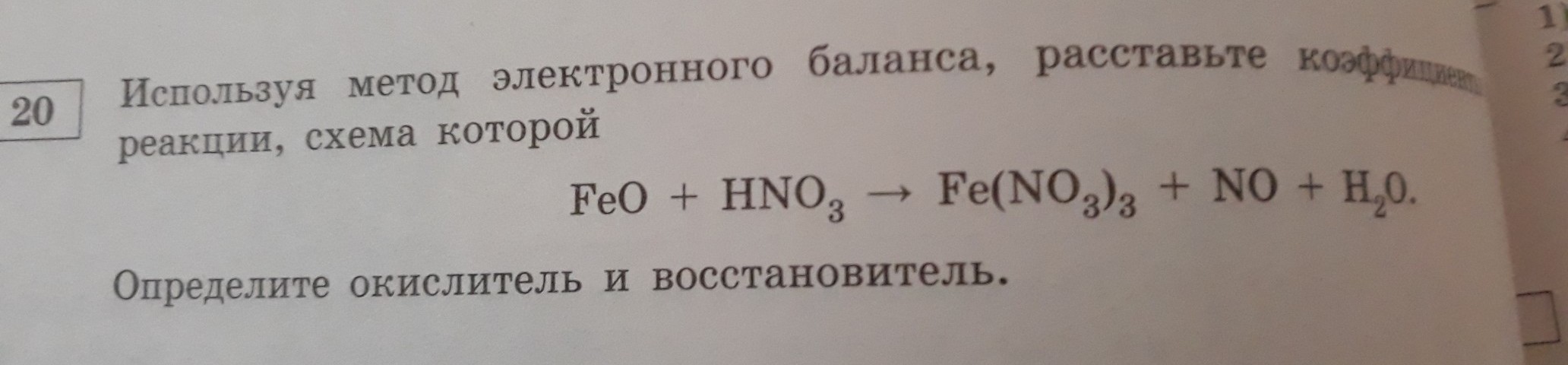
Ответы
Автор ответа:
0
Алгоритм решения :
Вычисляем изменение степени окисления каждого элемента в уравнении химической реакции .Выбираем только те элементы, которые поменяли степень окисления.Для найденных элементов составляем электронный баланс, заключающийся в подсчете количества приобретенных или отданных электронов.Находим наименьшее общее кратное для переданных электронов.Полученные значения и есть коэффициенты в уравнении
Вычисляем изменение степени окисления каждого элемента в уравнении химической реакции .Выбираем только те элементы, которые поменяли степень окисления.Для найденных элементов составляем электронный баланс, заключающийся в подсчете количества приобретенных или отданных электронов.Находим наименьшее общее кратное для переданных электронов.Полученные значения и есть коэффициенты в уравнении
Автор ответа:
1
1) Проставляем степени окисления всех элементов и смотрим, какие элементы меняют степени окисления в ходе реакции.
2) На основании этого составляем электронный баланс
Fe(+2) - 1e = Fe(+3) | 3 | восстановитель
N (+5) + 3e = N(+2) | 1 I окислитель
3) Значит у соединения NO ставим коэффициент 1, а у соединения FeO - коэффициент 3. И уравниваем остальные.
Получаем:
3FeO + 10HNO3 = 3Fe(NO3)3 + NO + 5H2O
2) На основании этого составляем электронный баланс
Fe(+2) - 1e = Fe(+3) | 3 | восстановитель
N (+5) + 3e = N(+2) | 1 I окислитель
3) Значит у соединения NO ставим коэффициент 1, а у соединения FeO - коэффициент 3. И уравниваем остальные.
Получаем:
3FeO + 10HNO3 = 3Fe(NO3)3 + NO + 5H2O
Turpal15:
а как нужно уравнивать? Я не умею
)-:
Похожие вопросы
Предмет: Английский язык,
автор: hanumarifova40
Предмет: Алгебра,
автор: ivlevaleksandr
Предмет: География,
автор: ramazanova2007
Предмет: Химия,
автор: tuleidanil
Предмет: Информатика,
автор: LENYCBKA61