Предмет: Алгебра,
автор: latasukap2mdat
Решите систему уравнений 9 класса
Приложения:

Ответы
Автор ответа:
0
Решение на уровне
Удачи
Удачи
Приложения:

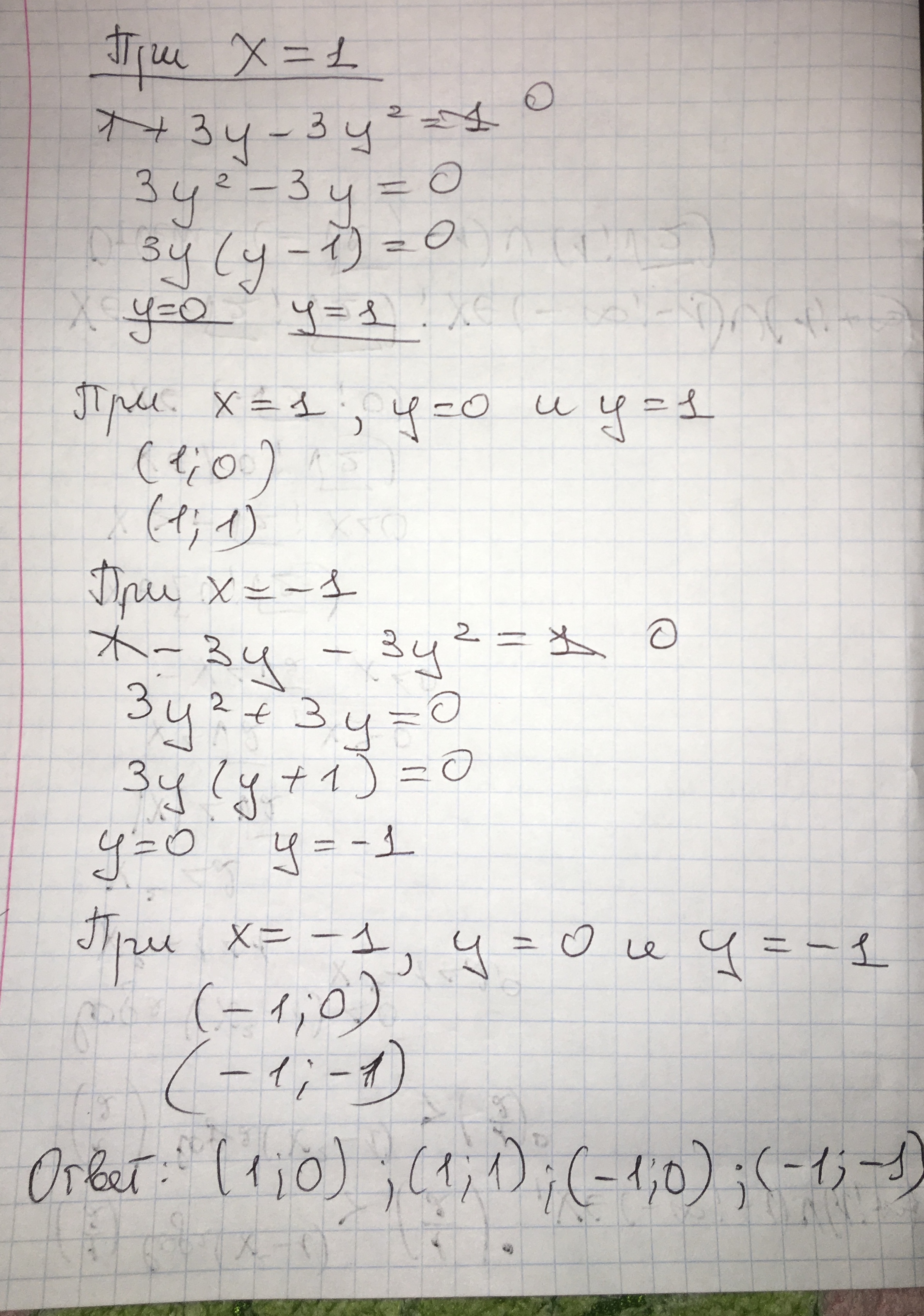
Автор ответа:
0
Извините, не заметил что не скинул вторую часть
Автор ответа:
0
Домножим первое уравнение на 2

Так как правые части равны, то левые можно приравнять

Получаем две системы (возьмём одно уравнение из совокупности, а другое - любое из исходной системы):
 ИЛИ
ИЛИ 
Ответ: (1; 0), (-1; 0), (1; 1), (-1; -1)
Так как правые части равны, то левые можно приравнять
Получаем две системы (возьмём одно уравнение из совокупности, а другое - любое из исходной системы):
Ответ: (1; 0), (-1; 0), (1; 1), (-1; -1)
Приложения:

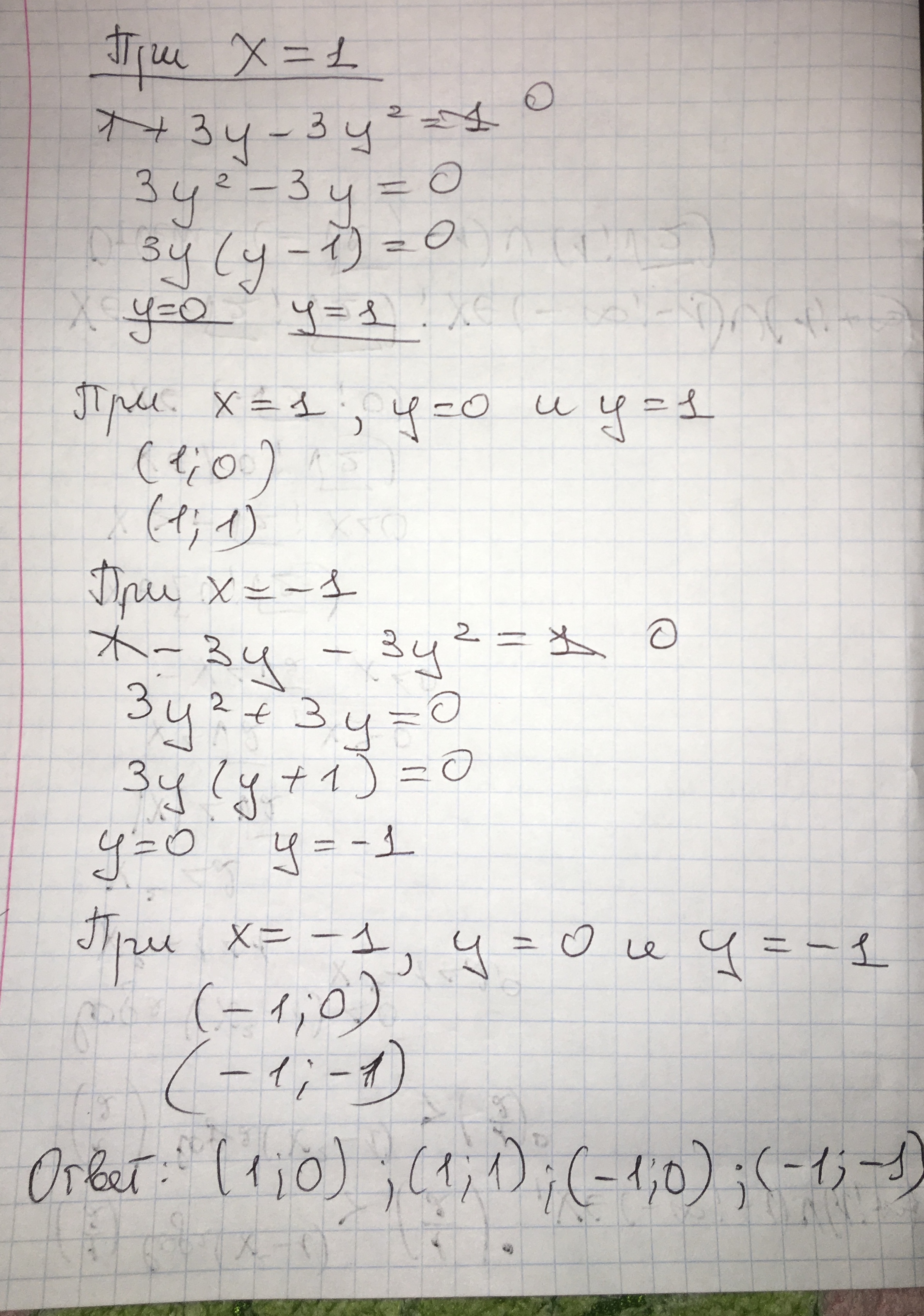
Похожие вопросы
Предмет: Русский язык,
автор: udovenkosofia12
Предмет: Биология,
автор: ProBroKrutoy48
Предмет: Химия,
автор: ekbdbekajshhsajjs
Предмет: География,
автор: валя141424
Предмет: Математика,
автор: irishka1609