Предмет: Химия,
автор: Аноним
Какова масса оксида взаимодействии с кислородом 5.4 г алюминия ? Какой объем кислорода израсходовался?
Ответы
Автор ответа:
0
4Al +3O2=2Al2O3
1)n(AL)=5.4 г/27г/моль=0.2 моль
2)n(Al2O3)=0.5n(Al)=0.1моль
n(O2)=4/3n(Al)=0.075моль
3)m(Al2O3)=0.1моль x 102г/моль=10.2г
Mr(Al2O3)=102г/моль
V(O2)=0.075моль x 22.4л/моль=1.68 л
Если помог нажми кнопку Спасибо)))
-Внизу приложил формулы по которым считал-
1)n(AL)=5.4 г/27г/моль=0.2 моль
2)n(Al2O3)=0.5n(Al)=0.1моль
n(O2)=4/3n(Al)=0.075моль
3)m(Al2O3)=0.1моль x 102г/моль=10.2г
Mr(Al2O3)=102г/моль
V(O2)=0.075моль x 22.4л/моль=1.68 л
Если помог нажми кнопку Спасибо)))
-Внизу приложил формулы по которым считал-
Приложения:
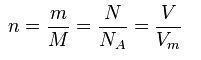
Автор ответа:
0
Спасибо
Автор ответа:
0
Не за что))
Похожие вопросы
Предмет: Другие предметы,
автор: memasiki2003
Предмет: Физика,
автор: danii2777
Предмет: Английский язык,
автор: Violetta20102
Предмет: Биология,
автор: YaroslavnaSmail
Предмет: Математика,
автор: Ochechel86