Предмет: Химия,
автор: 26Регинка
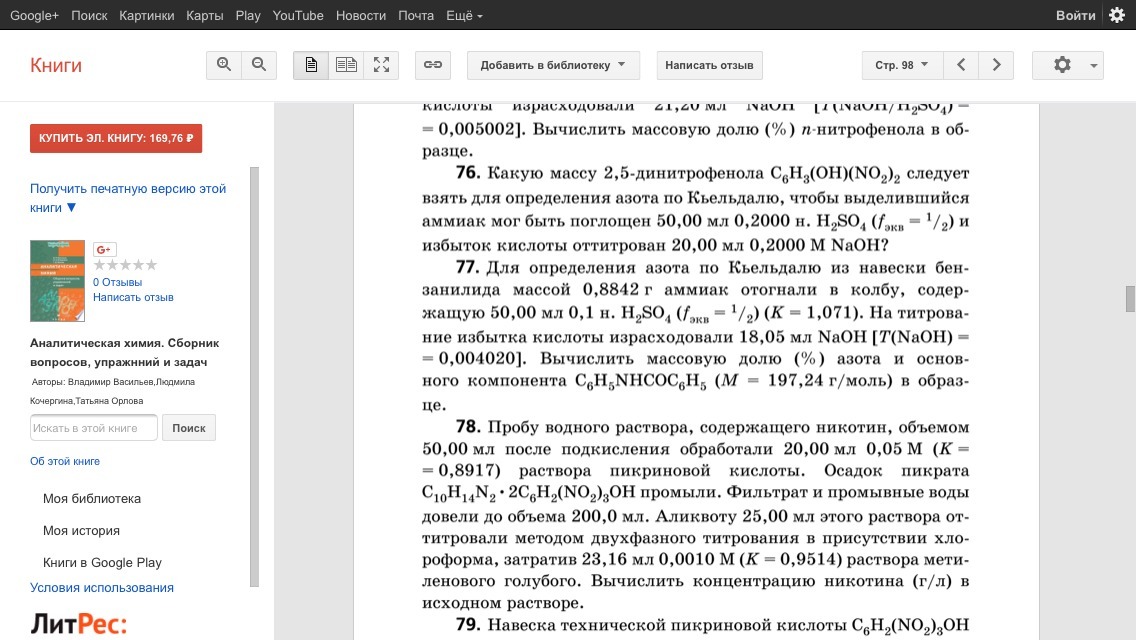
Помогите решить задачу 77
Приложения:

Ответы
Автор ответа:
0
NH₃ + H₂SO₄ = NH₄HSO₄ + H₂O
2NaOH + H₂SO₄ = Na₂SO₄ + 2H₂O
n(NaOH)=Tv(NaOH)/M(NaOH)
n(NaOH)=0,001859 моль
T=0,004020 г/мл
n(H₂SO₄)=v(H₂SO₄)N(H₂SO₄)f
f=1/2
n(H₂SO₄)=0,0025 моль
избыток кислоты
n’(H₂SO₄)=0,001859/2=0,0009295 моль
тогда на реакцию с аммиаком
n’’(H₂SO₄)=0,0015705 моль
n(NH₃)=n(N)=0,0015705 моль
w(N)=m(N)/m=n(N)M(N)/m
w(N)=0,02488 (2,488%)
массовая доля основного компонента
w=0,0015705*197,24/0,8842=0,3503 (35,03%)
Похожие вопросы
Предмет: Геометрия,
автор: Bebra0tyan
Предмет: Математика,
автор: skjfhdhd
Предмет: Биология,
автор: ignatenkoalina08
Предмет: Математика,
автор: aleksandertsyb