Предмет: Химия,
автор: AksLOL
3,2 г углеводорода сожгли и получили 9,9 г углекислого газа и 4,5г воды, D по водороду=64.
Решите пожалуйста, подробно объясняя все действия. Особенно как образовывается простейшая формула.
Ответы
Автор ответа:
0
3,2 г углеводорода сожгли и получили 9,9 г углекислого газа и 4,5г воды, D по водороду=64.
Приложения:
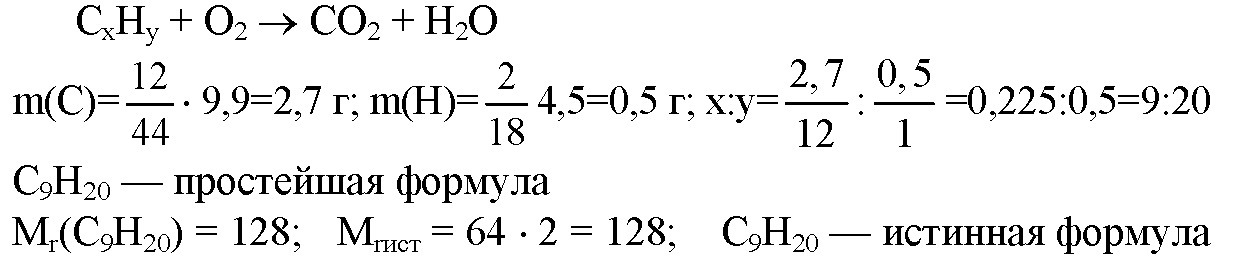
Автор ответа:
0
а как из 0,225:0,5 получается 9:20?
Автор ответа:
0
блин, не проснулся, что попало написал, сейчас исправил.
составим уравнение горения углеваодорода
3.2г 9,9 г 4,5 г
СхHy + O2 = CO2 + H2O
1. находим относительную молекулярную углеводорода (умножаем относительную плотность на относительную молекулярную массу водорода)
M(СхНy)=D*M(H2) = 64*2=128
найдем массы элементов
m(С) = 9.9*12/44 = 2.7г
m(H)=4.5*2/18 = 0.5г
найдем массовые доли элементов в углеводороде
w(C)=0.27/3.2 = 0.84375
w(H) = 0.5 / 3.2 = 0.15625
Найдем число атомов
N=w*M/Ar
N(C) = 0.84375*128/12 = 9
N(H) = 0.15625 * 128 / 1 = 20
C9H20
составим уравнение горения углеваодорода
3.2г 9,9 г 4,5 г
СхHy + O2 = CO2 + H2O
1. находим относительную молекулярную углеводорода (умножаем относительную плотность на относительную молекулярную массу водорода)
M(СхНy)=D*M(H2) = 64*2=128
найдем массы элементов
m(С) = 9.9*12/44 = 2.7г
m(H)=4.5*2/18 = 0.5г
найдем массовые доли элементов в углеводороде
w(C)=0.27/3.2 = 0.84375
w(H) = 0.5 / 3.2 = 0.15625
Найдем число атомов
N=w*M/Ar
N(C) = 0.84375*128/12 = 9
N(H) = 0.15625 * 128 / 1 = 20
C9H20
Приложения:
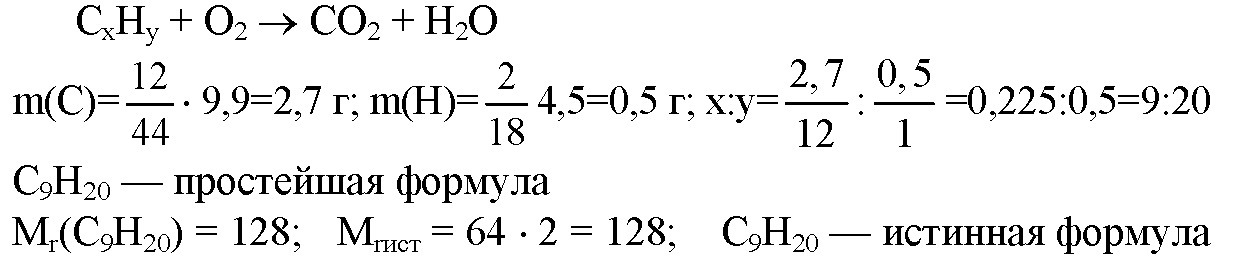
Автор ответа:
0
Вот только C9H20 должно получится
Автор ответа:
0
ага, так оно и есть, испарвил уже
Автор ответа:
0
Задача верная, получается С9Н20 без округлений n(C):n(H)=1:2.22...=9:20 Простейшая формула С9Н20 с учетом молярной массы, вычисленной по простейшей формуле и по относительной плотности по водороду, является истинной.
Похожие вопросы
Предмет: География,
автор: ramazanovaaruka870
Предмет: Математика,
автор: Аноним
Предмет: История,
автор: riavikto8
Предмет: Литература,
автор: dimazavodnikov