Предмет: Химия,
автор: 1235532
С1
Напишите уравнение реакций, с помощью которых можно осуществить следующие превращения:
Ba → BaO → Ba(OH)2 → BaCL2
Для первой реакции составьте схему электронного баланса, для 3 - ей реакции ионные уравнения реакция
-----------------------------------------------------------------------------------------------------------------------
С2
Определите массу соли (сульфида натрия), образующийся при взаимодействии 69г натрия с серой. Запишите полное решения задачи
Ответы
Автор ответа:
0
С1
Сейчас скину ионные.
Сейчас скину ионные.
Приложения:
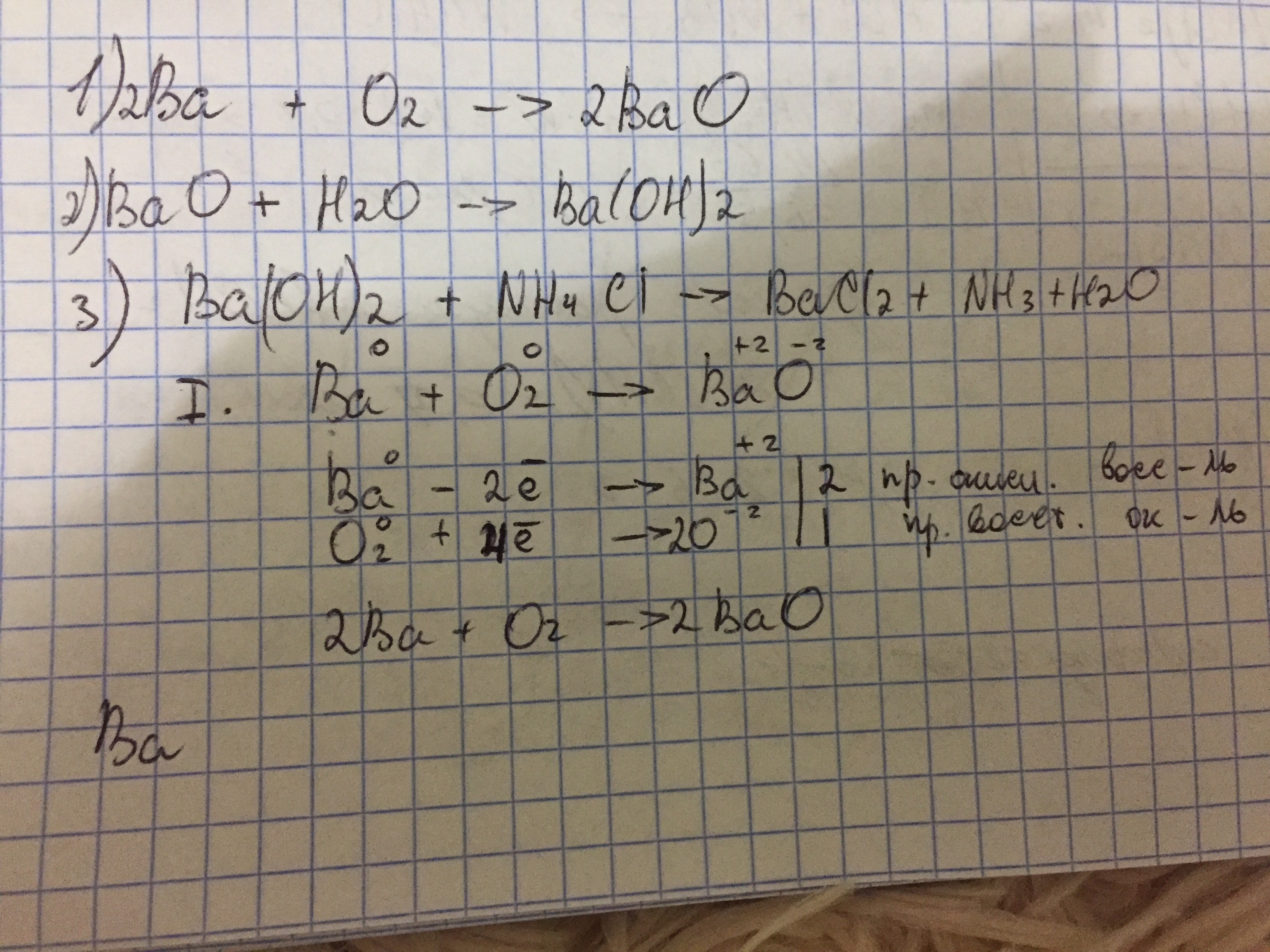
Автор ответа:
0
Ba(2+)+2OH(-)+NH4(+)+Cl(-)=Ba(2+)+2Cl(-)+NH3+H20
Автор ответа:
0
Сокращённое:
Автор ответа:
0
ааа, неправильно написала.
Автор ответа:
0
2Ba + O2 = 2BaO
BaO + H2O = Ba(OH)2
Ba(OH)2 + CuCl2 = BaCl2 + Cu(OH)2
Для первой:
Ba(0) - 2e = Ba(2+) | •2
O2(0) + 4e = 2O(2-) | •1
Для третьей:
Ba(2+) + 2OH(-) + Cu(2+) + 2Cl(-) = Ba(2+) + 2Cl(-) + Cu(OH)2
2OH(-) + Cu(2+) = Cu(OH)2
2Na + S = Na2S
1) n(Na) = 69/23 = 3 (моль)
2) n(Na) : n(Na2S) = 2 : 1 => n(Na2S)= 3:2 = 1,5
3) m(Na2S) = 1,5 + (46 + 32) = 117 (г)
Ответ: m (Na2S) = 117 г.
BaO + H2O = Ba(OH)2
Ba(OH)2 + CuCl2 = BaCl2 + Cu(OH)2
Для первой:
Ba(0) - 2e = Ba(2+) | •2
O2(0) + 4e = 2O(2-) | •1
Для третьей:
Ba(2+) + 2OH(-) + Cu(2+) + 2Cl(-) = Ba(2+) + 2Cl(-) + Cu(OH)2
2OH(-) + Cu(2+) = Cu(OH)2
2Na + S = Na2S
1) n(Na) = 69/23 = 3 (моль)
2) n(Na) : n(Na2S) = 2 : 1 => n(Na2S)= 3:2 = 1,5
3) m(Na2S) = 1,5 + (46 + 32) = 117 (г)
Ответ: m (Na2S) = 117 г.
Приложения:
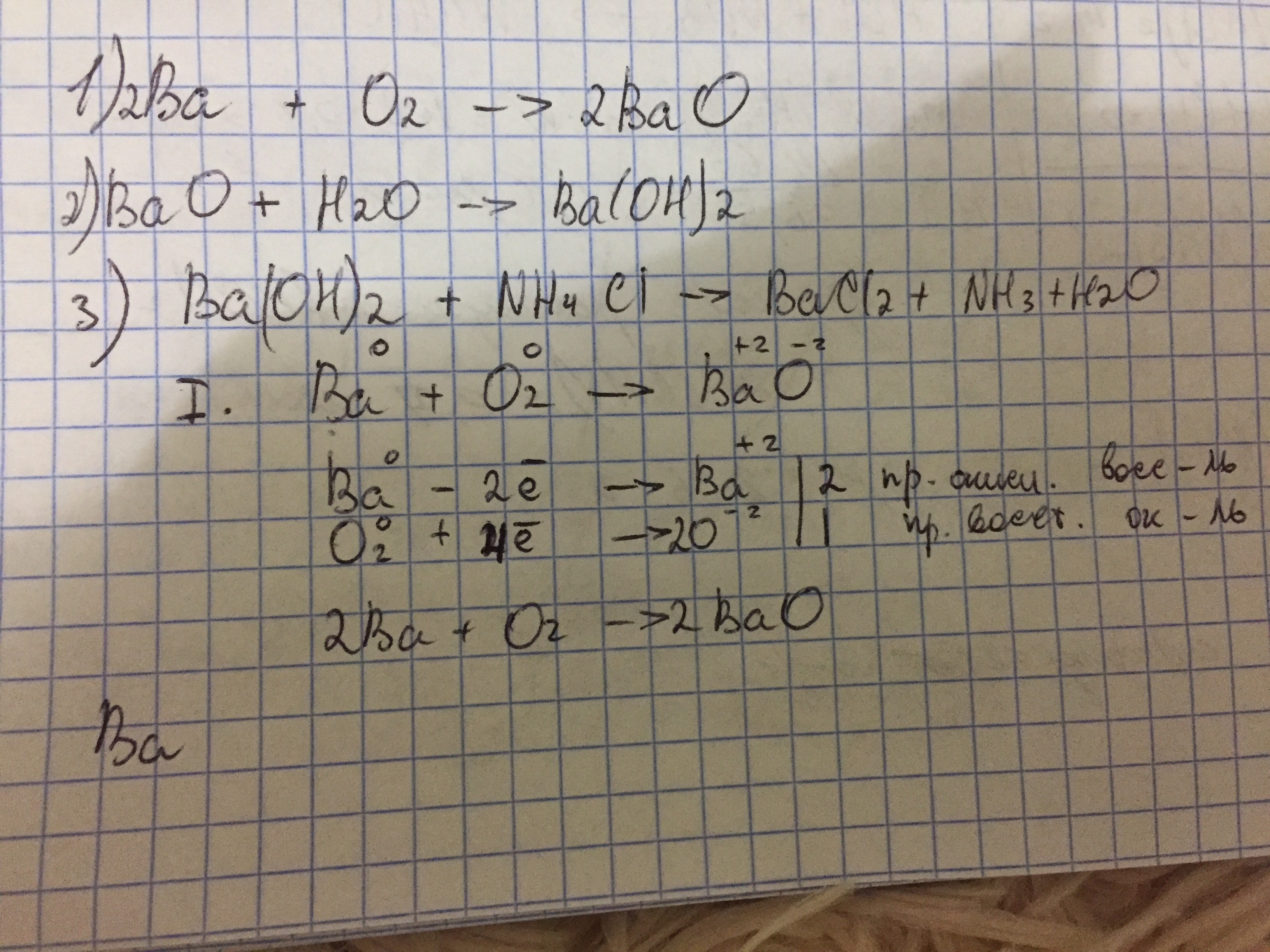
Похожие вопросы
Предмет: Математика,
автор: saulealimbekova946
Предмет: Литература,
автор: vikakovcyniak
Предмет: Русский язык,
автор: debilmisha
Предмет: Литература,
автор: новичок176
Предмет: Биология,
автор: SooJung