Предмет: Химия,
автор: Единoрог
(Задачи на избыток,с полным решением)
1.К раствору,содержащий 0,68 г хлорида цинка прилили раствор,содержащий 1,5г нитрата серебра(I). Вычислите массу веществ,находящихся в растворе по окончанию реакции.
2.Какая масса 8% раствора гидроксида натрия потребуется для полной нейтрализации 60г 5% раствора бромоводородной кислоты?
3.(фотография) там нужно подставить что-то, например ZnCl2+____=Zn(NO3)2+___
Помогите,пожалуйста!!
Приложения:
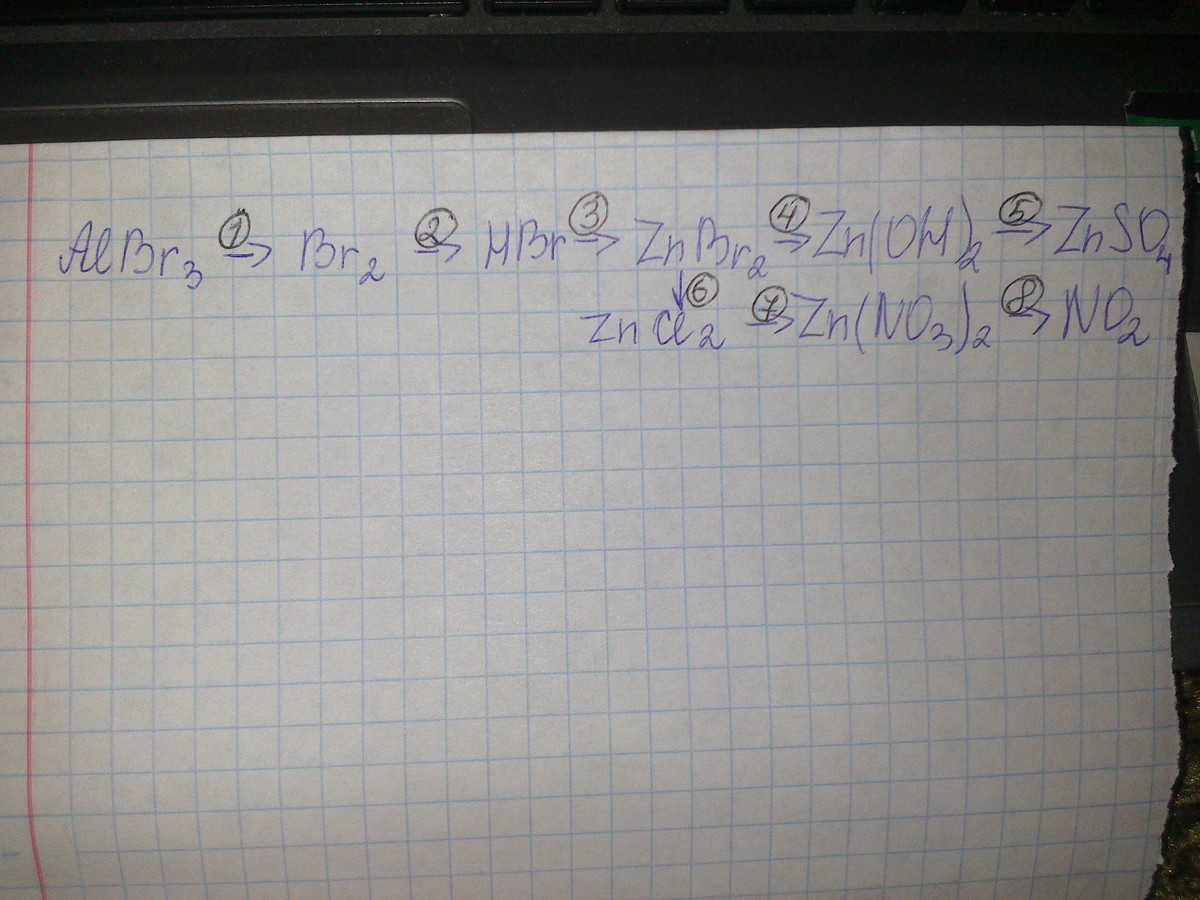
Ответы
Автор ответа:
0
ZnCl2 + 2AgNO3 = Zn(NO3)2+2AgCl
1 моль 2 моль
количество ZnCl2 = m/M = 0,68/136 =0,005моль
количество AgNO3 = 1,5 /170 =0,009моль
по уравнению реакции нитрата серебра в 2 раза больше,
следовательно на 0,009 мольл нитрата должно приходиться 0,0045 моль хлорида. (а у нас 0,005) следовательно хлорид в избытке, расчет по недостатку - нитрату серебра.
В растовре после реакции будут хлорид цинка (непрореагировавший = 0,005-0,0045 = 0,0005моль, нитрат цинка его кол-во = 0,0045 моль. хлоид серебра выпадет в осадок, поэтому в расторе его не будет)
масса хлорида цинка = 0,0005 моль * 136=0,068г
масса нитрата цинка = 0,0045*189=0,8505г
масса веществ в растворе = 0,068+0,8505=0,9185
2 задача
масса бромоводорода = массовая доля * массу растора = 0,05*60=3г
NaOH + HBr = NaBr + H2O
одномолярные отношения
кол-во бромоводорода = масса / молярную массу = 3/81 =0,037моль
т.к. отношения одномолярные, то и щелочи = 0,037 моль
масса щелочи = кол-во * молярную массу = 0,037*40=1,48г
масса растора щелочи = масса / массовую долю = 1,48/0,08=18,5г
3 задача
2AlBr3 + 3Cl2 = 2AlCl3 + 3Br2
Br2 + H2 = 2HBr
2HBr + Zn = ZnBr2 + H2
ZnBr2 + 2NaOH = Zn(OH)2 + 2NaBr
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
ZnBr2 + Cl2 = ZnCl2 + Br2
ZnCl2 + 2AgNO3 = Zn(NO3)2 + 2AgCl
2Zn(NO3)2 = 2ZnO + 4NO2 + O2 разложение при нагревании
1 моль 2 моль
количество ZnCl2 = m/M = 0,68/136 =0,005моль
количество AgNO3 = 1,5 /170 =0,009моль
по уравнению реакции нитрата серебра в 2 раза больше,
следовательно на 0,009 мольл нитрата должно приходиться 0,0045 моль хлорида. (а у нас 0,005) следовательно хлорид в избытке, расчет по недостатку - нитрату серебра.
В растовре после реакции будут хлорид цинка (непрореагировавший = 0,005-0,0045 = 0,0005моль, нитрат цинка его кол-во = 0,0045 моль. хлоид серебра выпадет в осадок, поэтому в расторе его не будет)
масса хлорида цинка = 0,0005 моль * 136=0,068г
масса нитрата цинка = 0,0045*189=0,8505г
масса веществ в растворе = 0,068+0,8505=0,9185
2 задача
масса бромоводорода = массовая доля * массу растора = 0,05*60=3г
NaOH + HBr = NaBr + H2O
одномолярные отношения
кол-во бромоводорода = масса / молярную массу = 3/81 =0,037моль
т.к. отношения одномолярные, то и щелочи = 0,037 моль
масса щелочи = кол-во * молярную массу = 0,037*40=1,48г
масса растора щелочи = масса / массовую долю = 1,48/0,08=18,5г
3 задача
2AlBr3 + 3Cl2 = 2AlCl3 + 3Br2
Br2 + H2 = 2HBr
2HBr + Zn = ZnBr2 + H2
ZnBr2 + 2NaOH = Zn(OH)2 + 2NaBr
Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O
ZnBr2 + Cl2 = ZnCl2 + Br2
ZnCl2 + 2AgNO3 = Zn(NO3)2 + 2AgCl
2Zn(NO3)2 = 2ZnO + 4NO2 + O2 разложение при нагревании
Похожие вопросы
Предмет: Русский язык,
автор: abdurahman12
Предмет: Биология,
автор: hnp7kfj9e4
Предмет: Қазақ тiлi,
автор: firsova78
Предмет: История,
автор: pauk2013