Предмет: Химия,
автор: 120520162017
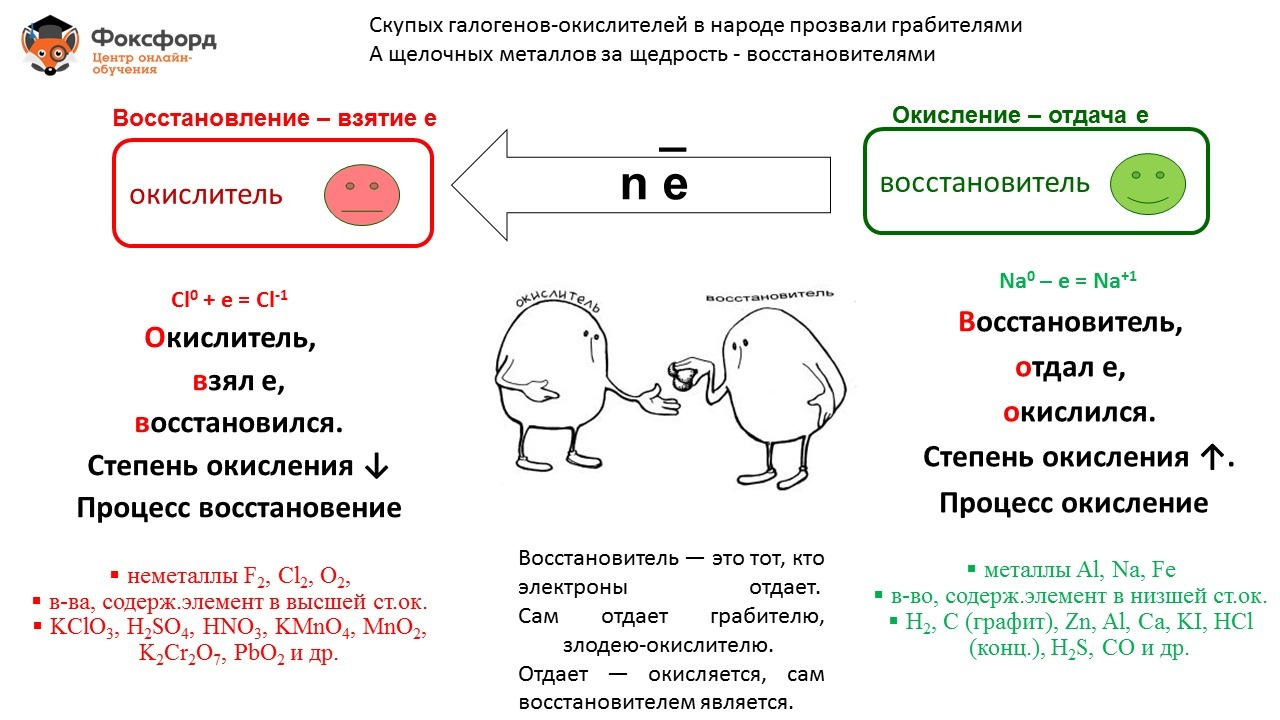
Реакции, в которых происходит изменение степеней окисления атомов элементов, входящих в состав реагирующих соединений называются окислительно - восстановительными.
В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим. Процесс отдачи электронов - окисление. При окислении степень окисления элемента повышается. Процесс присоединения электронов - восстановление, при этом степень окисления понижается.
Исходя из определения окислительно-восстановительного процесса, определите какие реакции невозможны:
C+H2O→H2CO3
S+H2SO4→H2S+H2O
NH3+O2→NO+H2O
Cl2+NaOH→NaCl+NaClO3+H2O
Na2O2+CO2=Na2CO3+O2
Приложения:
Ответы
Автор ответа:
0
С точки зрения окислительно-восстановительного процесса,все реакции (за исключением 2 и 4-ой) будут невозможны,так как элементы не меняют степени окисления или меняет только один элемент степень окисления,а для ОВР нужно,чтобы поменяли 2 элемента свои степени окисления.
(а если не с точки зрения ОВР рассматривать реакции,то все они возможны(правда продукт первой и второй неправильно записан)!)
(а если не с точки зрения ОВР рассматривать реакции,то все они возможны(правда продукт первой и второй неправильно записан)!)
Похожие вопросы
Предмет: Химия,
автор: melnikartem17
Предмет: Математика,
автор: ghhbnh
Предмет: Геометрия,
автор: vyacheslav9990
Предмет: Алгебра,
автор: ВадимЗинчук
Предмет: Математика,
автор: мАТЕМАТИКО