Предмет: Химия,
автор: kalyaev2000
какая масса гидроксида натрия должна вступить в реакцию с муравьиной кислотой, чтобы получилось 6.8г формиата натрия?
Ответы
Автор ответа:
0
NaOH + HCOOH = HCOONa + H2O
n формиат = m/M = 6,8 г/ 68 г/моль = 0,1 моль
m гидр.натр. = n*M = 0,1 моль* 40 г/моль = 4 г
n формиат = m/M = 6,8 г/ 68 г/моль = 0,1 моль
m гидр.натр. = n*M = 0,1 моль* 40 г/моль = 4 г
Автор ответа:
0
мой вариант решения ниже в фото
Приложения:
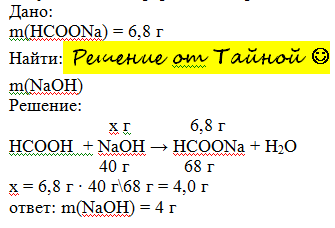
Похожие вопросы
Предмет: Биология,
автор: Аноним
Предмет: География,
автор: aldibaldiyar
Предмет: Математика,
автор: altynbekulydaniar3
Предмет: Математика,
автор: Аноним
Предмет: Математика,
автор: noname19981