Предмет: Химия,
автор: kcenia2010
Составьте электронный баланс
Приложения:
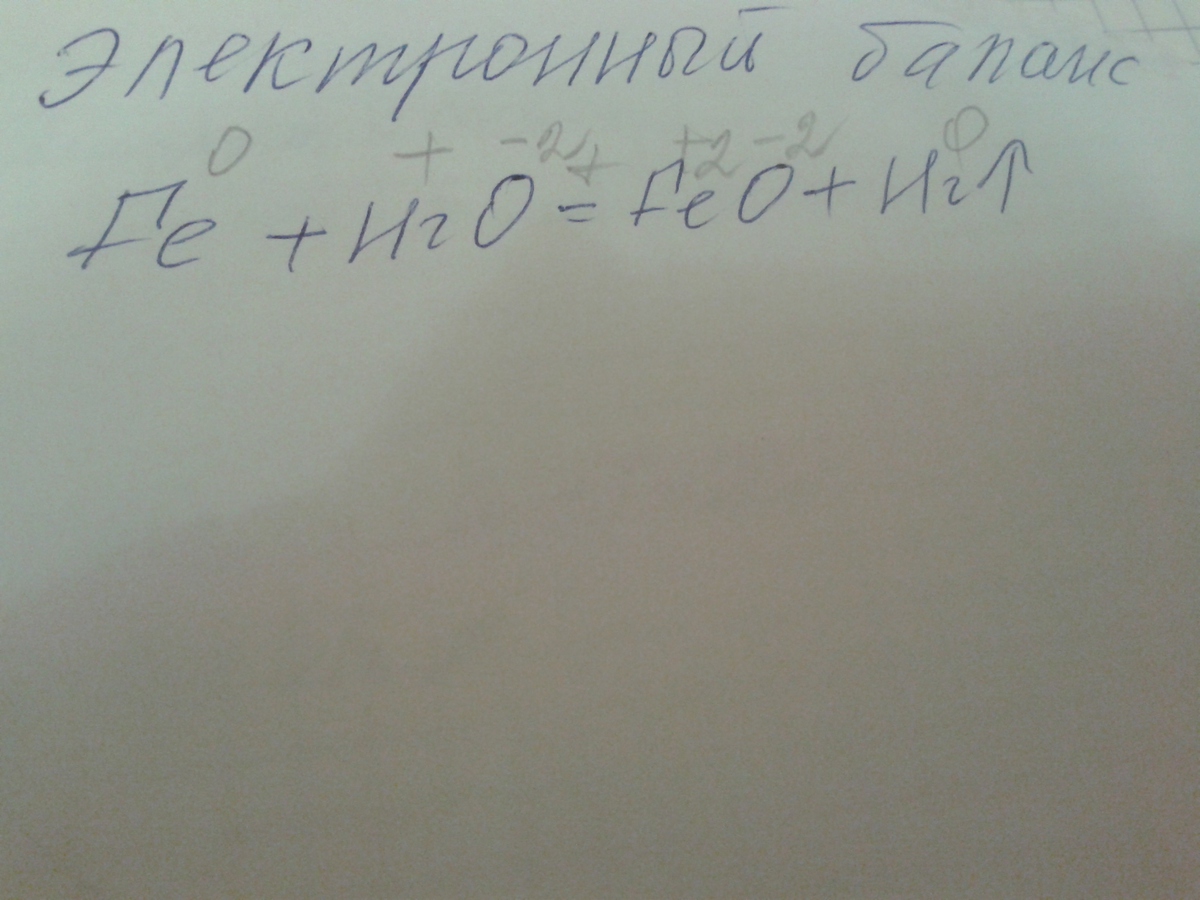
Ответы
Автор ответа:
0
H2(0) - 2e = 2H(+). 2. 1 окисление восстановитель
2
Fe(+2) + 2e = Fe(0). 2. 1 восстановление окислитель
2
Fe(+2) + 2e = Fe(0). 2. 1 восстановление окислитель
Автор ответа:
0
Fe + H²O => FeO + H². Расставляем коэффициенты в правую часть, тогда Fe со С.О. 0 отдает 2 электрона и переходит в Fe со С.О. +2, являясь при этом восстановителем (и окисляясь при этом). 2Н со С.О. +1 принимают по 1 электорону (то есть всего 2) и переходят в Н², являясь при этом окислителем (и восстанавливаясь при этом). Тогда коэффициенты равна 2 и 2, а значит, можно поделить на 2 и тогда в правой части уравнения реакции при продуктах будут единицы, то есть, коэффициенты не нужны, т.к. и так все сходится. Ответ: Fe + H²O => FeO + H².
Похожие вопросы
Предмет: Физика,
автор: d00546605
Предмет: История,
автор: skorobogatovanaksua
Предмет: История,
автор: sashashanova3
Предмет: Математика,
автор: syckovdima89
Предмет: Английский язык,
автор: Ggggra