Предмет: Химия,
автор: Alenakom99
какой объем спиртового раствора гидроксида натрия с массовой долей NaOH 8% (плотность 0,96г/мл) потребуется для дегидрохлорирования 2-хлорпропана массой 7,85 г?
Напишите пожалуйста подробное решение
Ответы
Автор ответа:
0
составим уравнение дегидрохлорирования
7.85g xg
СН3-СН(Сl)-СН3 + NaOH ⇒ CH2 =CH-CH3+NaOH+H2O
78.5g 40g
где 78.5 и 40 это молярные массы хлорпропана и гидроксида натрия по таблице Менделеева
x=7.85·40÷78.5=4g
теперь рассчитаем массу 100%-ого раствора по пропорции
4 г - 8%
х г - 100%
х=4×100÷8=50 г
теперь граммы переведем в мл по формуле V=m/ρ V=50/0.96=52.1 ml
7.85g xg
СН3-СН(Сl)-СН3 + NaOH ⇒ CH2 =CH-CH3+NaOH+H2O
78.5g 40g
где 78.5 и 40 это молярные массы хлорпропана и гидроксида натрия по таблице Менделеева
x=7.85·40÷78.5=4g
теперь рассчитаем массу 100%-ого раствора по пропорции
4 г - 8%
х г - 100%
х=4×100÷8=50 г
теперь граммы переведем в мл по формуле V=m/ρ V=50/0.96=52.1 ml
Автор ответа:
0
Решение данной задачи в
фото ниже
Приложения:
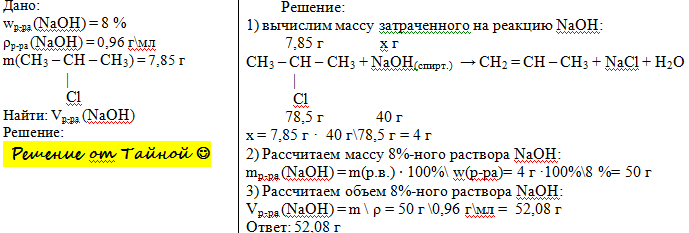
Похожие вопросы
Предмет: Русский язык,
автор: oksanasablina
Предмет: Английский язык,
автор: mashaillina2904
Предмет: Английский язык,
автор: rutat82
Предмет: Математика,
автор: fedotovrodion
Предмет: Биология,
автор: vovaskv