Предмет: Химия,
автор: abramenko2001
Некоторый элемент образует оксиды, содержащие 52,98% и 18,39% кислорода соответственно. Определите формулы оксидов и соответствующих им кислот.
Я даже составила систему, а решить ее не могу.
Приложения:
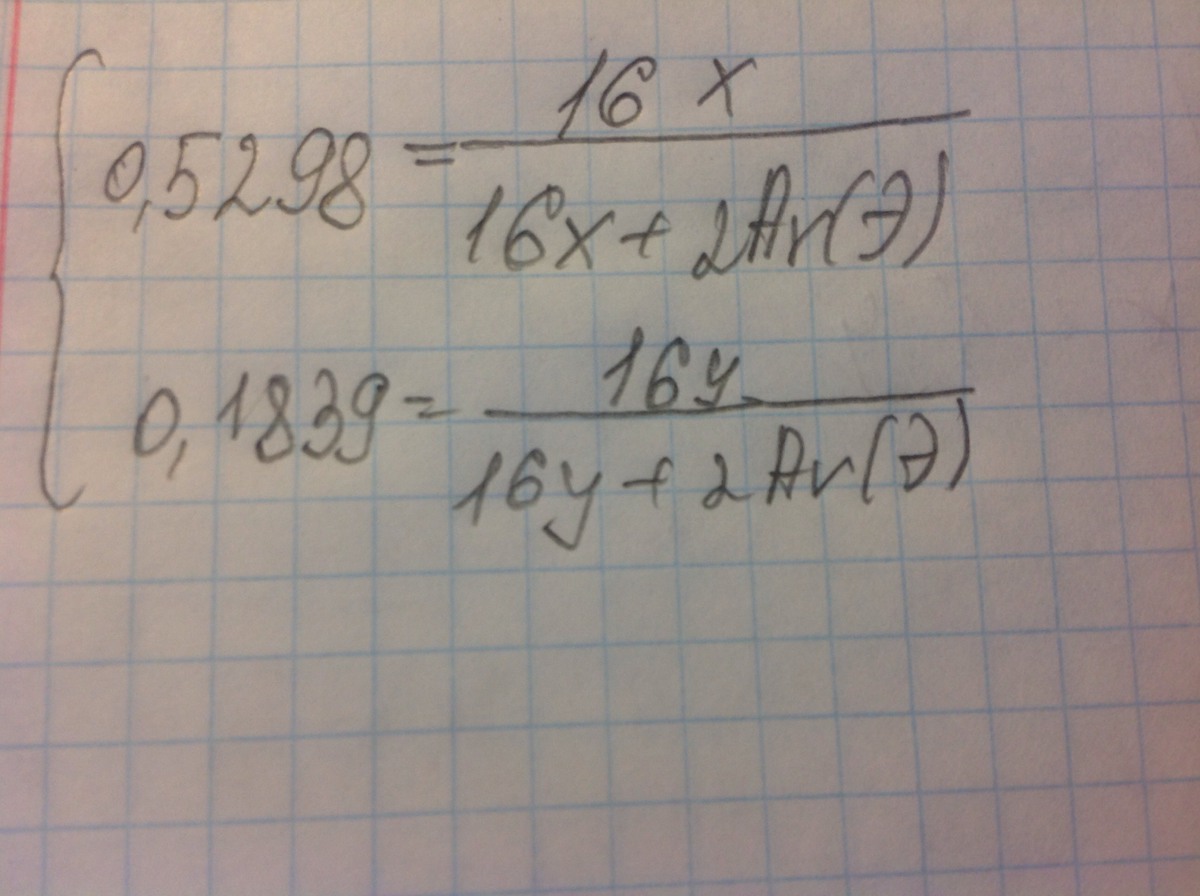
Ответы
Автор ответа:
10
Это у вас не система, это два разных уравнения.
Начнём во второго оксида. Массовая доля элемента в нём = 81,71 %
Далее по закону эквивалентов массовые доли элементов в оксиде относятся как их эквиваленты (эквивалент кислорода = 8)
18,38/81,71 = 8/х
х = 35,5. Этому условию соответствует элемент хлор, а оксид - Cl2O, кислота HClO.
Аналогично вычисляем по первому оксиду.
47,02/52,98 = х/8
х= 7,1, это в 5 раз меньше атомной массы хлора, значит, речь идёт об оксиде хлора (5) Cl2O5, кислота HClO3
Начнём во второго оксида. Массовая доля элемента в нём = 81,71 %
Далее по закону эквивалентов массовые доли элементов в оксиде относятся как их эквиваленты (эквивалент кислорода = 8)
18,38/81,71 = 8/х
х = 35,5. Этому условию соответствует элемент хлор, а оксид - Cl2O, кислота HClO.
Аналогично вычисляем по первому оксиду.
47,02/52,98 = х/8
х= 7,1, это в 5 раз меньше атомной массы хлора, значит, речь идёт об оксиде хлора (5) Cl2O5, кислота HClO3
abramenko2001:
только в ответах Бром
Нет ничего проще - проверочное решение! Mr(Cl2O5) = 151, массовая доля кислорода = 80/151*100 = 52,92
Второй оксид можете сами пересчитать))))
80*100%/151=52.98% твой ответ правильно
втором оксиде не совпадает чо то
16*100%/87=18.39 тоже ответ
Похожие вопросы
Предмет: Окружающий мир,
автор: Маринетте
Предмет: Русский язык,
автор: Юлианасасас
Предмет: Русский язык,
автор: LidiaGorbulko5390
Предмет: Литература,
автор: sergeymk06
Предмет: Английский язык,
автор: dulovaeva