Предмет: Химия,
автор: msnezka
рассчитайте массу водорода и химическое количество гидроксида натрия, которые образуются в результате взаимодействия натрия массой 4,60г. с избытком воды.... и ещё одна.....в раствор нитрата серебра массой 400 гр.с массовой долей соли 8,50% опустили избыток цинковых опилок. Определить массу серебра, выделившегося в результате химической реакции
msnezka:
а как в "Дано" написать массовой долей соли 8,50% ? соль тут где? и откуда 340г....
Ответы
Автор ответа:
0
и еще
2)34г хг
Zn+2AgNO3=Zn(NO3)2+2Ag
340г 216г
m (AgNO3) 2 в-ва = м р-ра*ω/100% = 400*8,5%/100%=34г
х=21,6г
2)34г хг
Zn+2AgNO3=Zn(NO3)2+2Ag
340г 216г
m (AgNO3) 2 в-ва = м р-ра*ω/100% = 400*8,5%/100%=34г
х=21,6г
Приложения:
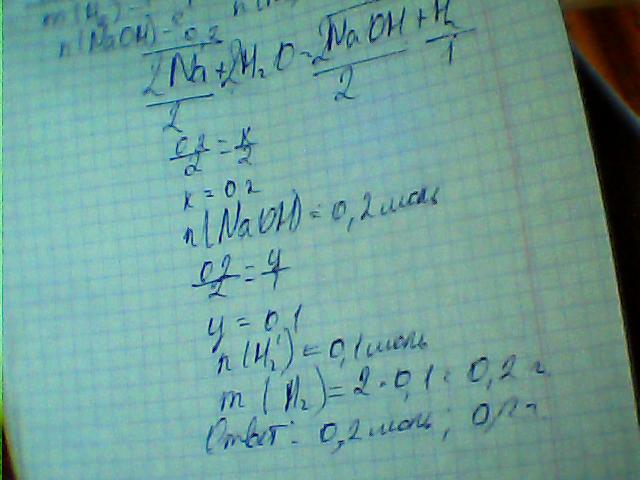
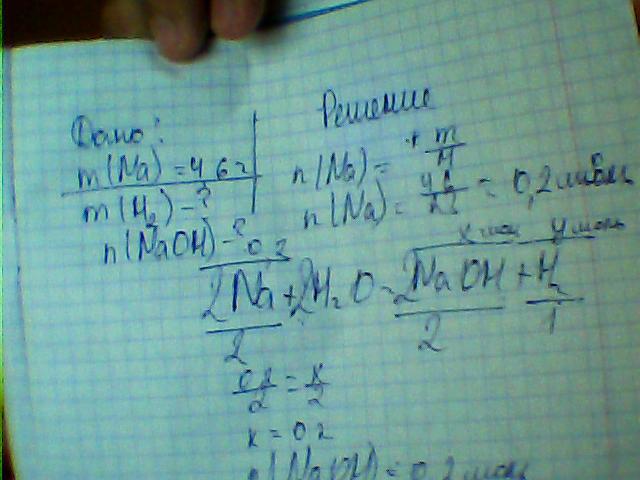
а как в "Дано" написать массовой долей соли 8,50% ? соль тут где?
W=8.50% m=400гр
Похожие вопросы
Предмет: Русский язык,
автор: Владик1234521345789
Предмет: Английский язык,
автор: tatiana0808
Предмет: Русский язык,
автор: mozaevaanastasi
Предмет: Химия,
автор: denberezhnij
Предмет: Алгебра,
автор: mixa1974