Предмет: Химия,
автор: ylikmir
1.Через 300мл 5%-ого раствора соляной к-ты (Р-1,1г/мл) пропустили 10 л хлороводорода. Рассчитайте %-ность получ. раствора кислоты.
NedNick:
Через соляную кислоту пропустили хлороводород! хахахаха
вот я и не пойму что за....
точно 10 литров хлороводорода
не МЛ?
возможно не правильно переписала
Если Л, то 97,23% выходит
а решение?
Ответы
Автор ответа:
1
блаблаблаблаблаблабла
Приложения:
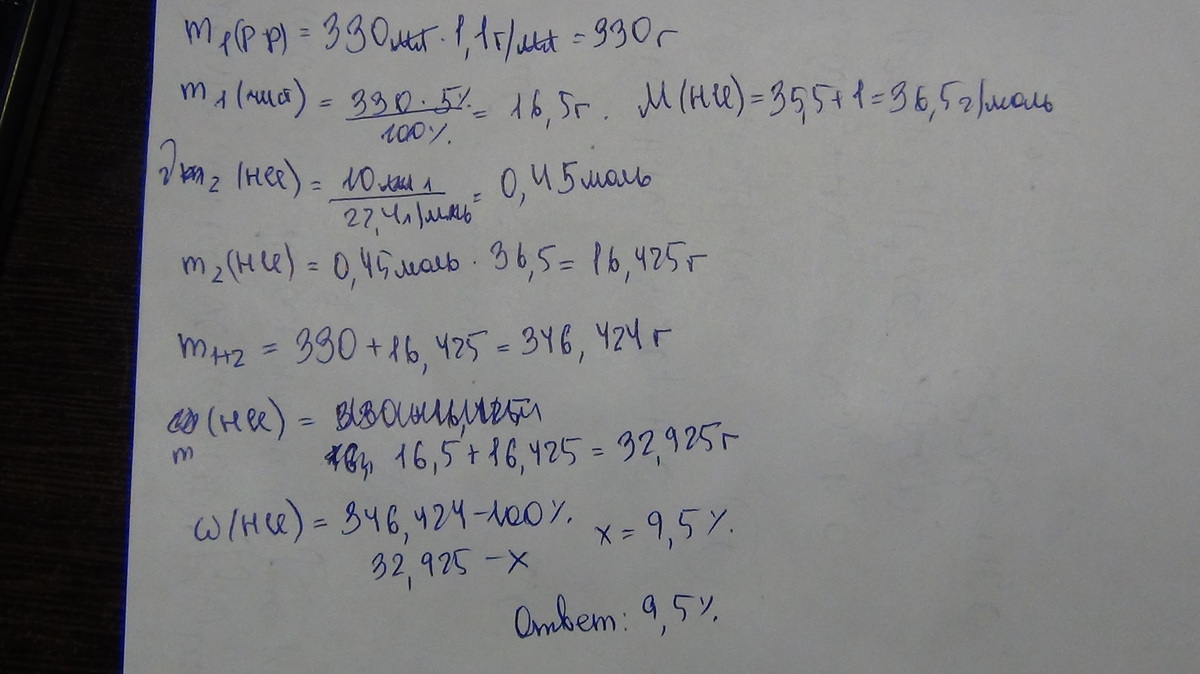
Спасибо)
От вашего решения волосы встают. Оно не верно
Да, оно неверно.
я считала для 10 мл. 10л слишком много
В условии было написано 10 литров, а я перевел в Мл
Посмотрите на задачу с практической точки зрения. как вы будете пропускать 10 л через 300мл=0.3 л???
Автор ответа:
1
масса первоначального раствора 300мл*1,1г/мл=330г.
масса НСI в нем 330*0,05=16.5г
10л хлороводорода это 10/22.4=0.45 моль
найдем массу 0.45*М( морярная масса HCI)= 0.45*36.5=16.425г
Получается, что в раствор добавили 16.425 г соляной кислоты( хророводород газ - а в жидком состоянии - соляная кислота)
Масса нового раствора 330+16.425=346.424г
массовая доля НСI= (16.5+16.425)/346.424=33/346.424=0.095 или 9.5%
масса НСI в нем 330*0,05=16.5г
10л хлороводорода это 10/22.4=0.45 моль
найдем массу 0.45*М( морярная масса HCI)= 0.45*36.5=16.425г
Получается, что в раствор добавили 16.425 г соляной кислоты( хророводород газ - а в жидком состоянии - соляная кислота)
Масса нового раствора 330+16.425=346.424г
массовая доля НСI= (16.5+16.425)/346.424=33/346.424=0.095 или 9.5%
Похожие вопросы
Предмет: Русский язык,
автор: Тупей
Предмет: Русский язык,
автор: Andrei861
Предмет: Русский язык,
автор: akzharkin12mm
Предмет: Физика,
автор: dagmaii1
Предмет: Немецкий язык,
автор: mast1323