Предмет: Химия,
автор: vvanya99
Вычислить массу эфира полученного при взаимодействии 10 г метановой кислоты и 8 г метанола.надо срочно!!!!
Ответы
Автор ответа:
1
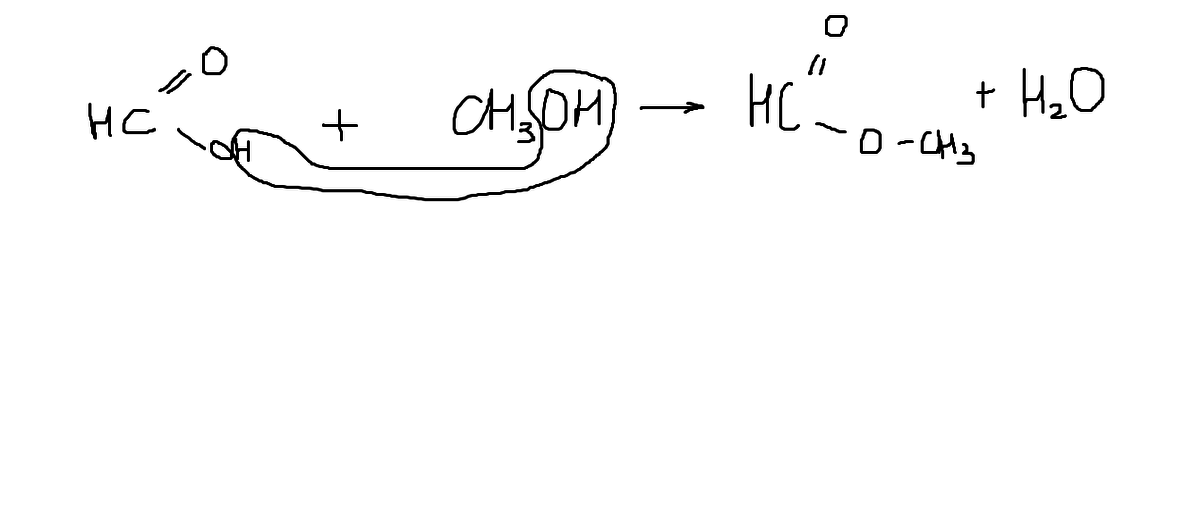
Уравнение в приложении
Дано:
m(СHOOH)=10г
m(CH3OH)=8г
Найти: m эфира - ? (г)
Решение:
n(HCOOH)= m/ M = 10г / (1+12+16+16+1) г/моль = 0,217 моль
n(CH3OH) = 8г / 32 г/моль = 0,25 моль
По уравнению все вещества в отношении 1:1
По логике здесь метанол в избытке, значит, массу будем считать по количеству метановой кислоты
m (CHOOCH3) = n*M= 0.217 моль * (12+1+16+16+12+3) г/моль = 0.217 моль * 60 г/моль = 13,02 г
Ответ: 13.02 г
Дано:
m(СHOOH)=10г
m(CH3OH)=8г
Найти: m эфира - ? (г)
Решение:
n(HCOOH)= m/ M = 10г / (1+12+16+16+1) г/моль = 0,217 моль
n(CH3OH) = 8г / 32 г/моль = 0,25 моль
По уравнению все вещества в отношении 1:1
По логике здесь метанол в избытке, значит, массу будем считать по количеству метановой кислоты
m (CHOOCH3) = n*M= 0.217 моль * (12+1+16+16+12+3) г/моль = 0.217 моль * 60 г/моль = 13,02 г
Ответ: 13.02 г
Приложения:
vvanya99:
Спасибо огромное
А почему в решении получилось 13.02,а в ответ пошло 32?
Я уже исправила, опечаталась :)
Аа,ну ясно)
А то я с химией совсем не дружу)
Поможешь ещё с одной задачей?
Похожие вопросы
Предмет: Окружающий мир,
автор: Jasmin2009
Предмет: Русский язык,
автор: НяшМилаш11
Предмет: Русский язык,
автор: po340
Предмет: Алгебра,
автор: anasteicha3
Предмет: География,
автор: karinam271106