Предмет: Химия,
автор: potroshitel099
помогите!!!срочно!!!пожалуйста!!!!!!
Приложения:


Ответы
Автор ответа:
2
Приветствую.
Задание 1.
С помощью NaOH.
1.С NaСl ( хлорид натрия ) реакция не идёт.
2. MgCl₂ + 2NaOH = Mg(OH)₂↓ +2NaCl ( образуется осадок, не растворим в избытке щёлочи)
Mg₂⁺ + 2Cl⁻ + 2Na⁺ + 2OH⁻ = Mg(OH)₂↓ + 2Na⁺ + 2Cl⁻
Mg²⁺ + 2OH⁻ = Mg(OH)₂↓
3. AlCl₃ + 3NaOH = Al(OH)₃↓ + 3NaCl ( образуется осадок, растворимый в избытке щёлочи)
Al³⁺ +3Cl⁻ + 3Na⁺ + 3OH⁻ = Al(OH)₃↓ + 3Na⁺ + 3Cl⁻
Al³⁺ + 3OH⁻ = Al(OH)₃↓
Al(OH)₃ + NaOH = Na[Al(OH)₄]
Задание 2.
Используем пробу на пламя.
NaCl + пламя = желтая окраска
KCl + пламя = фиолетовая окраска
CaCl₂ + пламя = кирпично-красная окраска
Задание 3.
FeSO₄ , в растворе имеет зеленый цвет.
Fe2(SO₄)₃, в растворе имеет желтый цвет.
CuSO₄ , сине-голубая окраска раствора.
Задание 4.
Для FeCl₃:
1. FeCl₃ + 3NaOH = 3NaCl + Fe(OH)₃↓ (осадок бурого цвета)
Fe³⁺ + 3Cl⁻ + 3Na⁺ + 3OH⁻ = 3Na⁺ +3Cl⁻ + Fe(OH)₃↓
Fe³⁺ + 3OH⁻ = Fe(OH)₃↓
2. FeCl₃ + 3AgNO₃ = Fe(NO₃)₃↓ + 3AgCl (осадок белого цвета)
Fe³⁺ + 3Cl⁻ + 3Ag⁺ + 3NO₃⁻ = Fe(NO₃)₃↓ + 3Ag⁺ + 3Cl⁻
Fe³⁺ + 3NO₃⁻ = Fe(NO₃)₃↓
Для FeSO₄:
1. FeSO₄ + 2NaOH = Na₂SO₄ + Fe(OH)₂↓ (осадок темно-зеленого цвета)
Fe²⁺ + SO₄²⁻ + 2Na⁺ + 2OH⁻ = 2Na⁺ + SO₄²⁻ + Fe(OH)₂↓
Fe²⁺ + 2OH⁻ = Fe(OH)₂↓
2. FeSO₄ + BaCl₂ = FeCl₂ + BaSO₄↓ (осадок белого цвета)
Fe²⁺ + SO₄²⁻ + Ba²⁺ + 2Cl⁻ = Fe²⁺ + 2Cl⁻ + BaSO₄↓
Ba²⁺ + SO₄²⁻ = BaSO₄↓
Задание 5.
Для определения примеси сульфата железа ( lll ) , в железном корпусе воспользуемся качественно реакцией на ион Fe³⁺ , т.е. проведём реакцию с желтой кровяной солью.
2Fe₂(SO₄)₃ + 3K₄[Fe(CN)⁶]₃↓ + 6K₂SO₄
Если примесь Fe³⁺ содержится в корпусе, то выпадает темно-синий осадок турнбулевой сини.
Задание 6.
В фото.
Задание 1.
С помощью NaOH.
1.С NaСl ( хлорид натрия ) реакция не идёт.
2. MgCl₂ + 2NaOH = Mg(OH)₂↓ +2NaCl ( образуется осадок, не растворим в избытке щёлочи)
Mg₂⁺ + 2Cl⁻ + 2Na⁺ + 2OH⁻ = Mg(OH)₂↓ + 2Na⁺ + 2Cl⁻
Mg²⁺ + 2OH⁻ = Mg(OH)₂↓
3. AlCl₃ + 3NaOH = Al(OH)₃↓ + 3NaCl ( образуется осадок, растворимый в избытке щёлочи)
Al³⁺ +3Cl⁻ + 3Na⁺ + 3OH⁻ = Al(OH)₃↓ + 3Na⁺ + 3Cl⁻
Al³⁺ + 3OH⁻ = Al(OH)₃↓
Al(OH)₃ + NaOH = Na[Al(OH)₄]
Задание 2.
Используем пробу на пламя.
NaCl + пламя = желтая окраска
KCl + пламя = фиолетовая окраска
CaCl₂ + пламя = кирпично-красная окраска
Задание 3.
FeSO₄ , в растворе имеет зеленый цвет.
Fe2(SO₄)₃, в растворе имеет желтый цвет.
CuSO₄ , сине-голубая окраска раствора.
Задание 4.
Для FeCl₃:
1. FeCl₃ + 3NaOH = 3NaCl + Fe(OH)₃↓ (осадок бурого цвета)
Fe³⁺ + 3Cl⁻ + 3Na⁺ + 3OH⁻ = 3Na⁺ +3Cl⁻ + Fe(OH)₃↓
Fe³⁺ + 3OH⁻ = Fe(OH)₃↓
2. FeCl₃ + 3AgNO₃ = Fe(NO₃)₃↓ + 3AgCl (осадок белого цвета)
Fe³⁺ + 3Cl⁻ + 3Ag⁺ + 3NO₃⁻ = Fe(NO₃)₃↓ + 3Ag⁺ + 3Cl⁻
Fe³⁺ + 3NO₃⁻ = Fe(NO₃)₃↓
Для FeSO₄:
1. FeSO₄ + 2NaOH = Na₂SO₄ + Fe(OH)₂↓ (осадок темно-зеленого цвета)
Fe²⁺ + SO₄²⁻ + 2Na⁺ + 2OH⁻ = 2Na⁺ + SO₄²⁻ + Fe(OH)₂↓
Fe²⁺ + 2OH⁻ = Fe(OH)₂↓
2. FeSO₄ + BaCl₂ = FeCl₂ + BaSO₄↓ (осадок белого цвета)
Fe²⁺ + SO₄²⁻ + Ba²⁺ + 2Cl⁻ = Fe²⁺ + 2Cl⁻ + BaSO₄↓
Ba²⁺ + SO₄²⁻ = BaSO₄↓
Задание 5.
Для определения примеси сульфата железа ( lll ) , в железном корпусе воспользуемся качественно реакцией на ион Fe³⁺ , т.е. проведём реакцию с желтой кровяной солью.
2Fe₂(SO₄)₃ + 3K₄[Fe(CN)⁶]₃↓ + 6K₂SO₄
Если примесь Fe³⁺ содержится в корпусе, то выпадает темно-синий осадок турнбулевой сини.
Задание 6.
В фото.
Приложения:
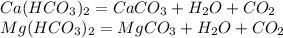
potroshitel099:
спасибо большое
да спасибо родная
Похожие вопросы
Предмет: Русский язык,
автор: машаш178
Предмет: Английский язык,
автор: micado
Предмет: Русский язык,
автор: maxtozhyn
Предмет: Математика,
автор: lksuhal