Предмет: Химия,
автор: DarkCastor
придумайте и решите задачу по формуле. оч срочно! пжлста
Приложения:
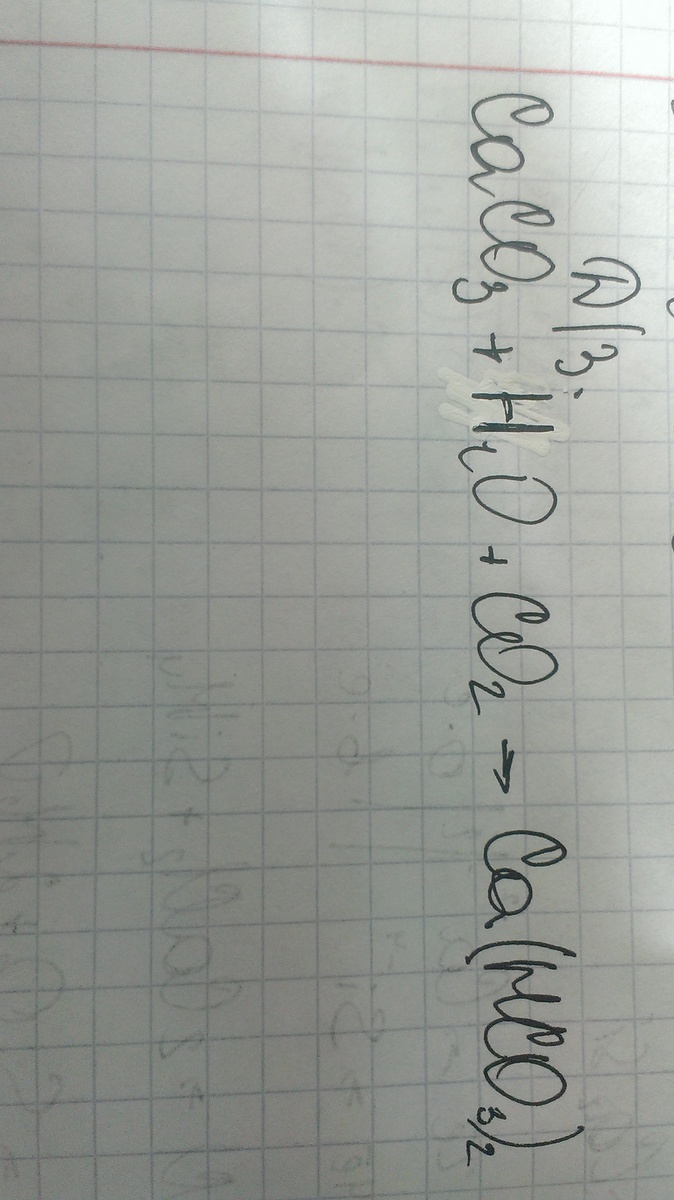
Ответы
Автор ответа:
1
Какова масса гидрокарбоната кальция, полученного при взаимодействии карбоната кальция, углекислого газа и 4.5 грамм воды?
Дано:
m(H2O)=4.5 г
Найти:
m(Ca(HCO3)2)=?
Решение:
CaCO3 + H2O + CO2 = Ca(HCO3)2
n(H2O)=m/M=4.5 г / 18 г/моль =0.25 моль
n(Ca(HCO3)2)=0.25 моль
m(Ca(HCO3)2)=M*n=162 г/моль * 0.25 моль = 40.5 г
Ответ: 40.5 г
Дано:
m(H2O)=4.5 г
Найти:
m(Ca(HCO3)2)=?
Решение:
CaCO3 + H2O + CO2 = Ca(HCO3)2
n(H2O)=m/M=4.5 г / 18 г/моль =0.25 моль
n(Ca(HCO3)2)=0.25 моль
m(Ca(HCO3)2)=M*n=162 г/моль * 0.25 моль = 40.5 г
Ответ: 40.5 г
DarkCastor:
спасибо
Похожие вопросы
Предмет: Другие предметы,
автор: 99999925
Предмет: Қазақ тiлi,
автор: ароьгүөһүам
Предмет: Українська література,
автор: Ксюшка789
Предмет: Математика,
автор: margo4092
Предмет: Другие предметы,
автор: saidkamol12