Предмет: Химия,
автор: akezha454
какое количество водорода выделится при взаимодействии 2.3 г. натрия серной кислотой поже побыстрее срочно
Приложения:
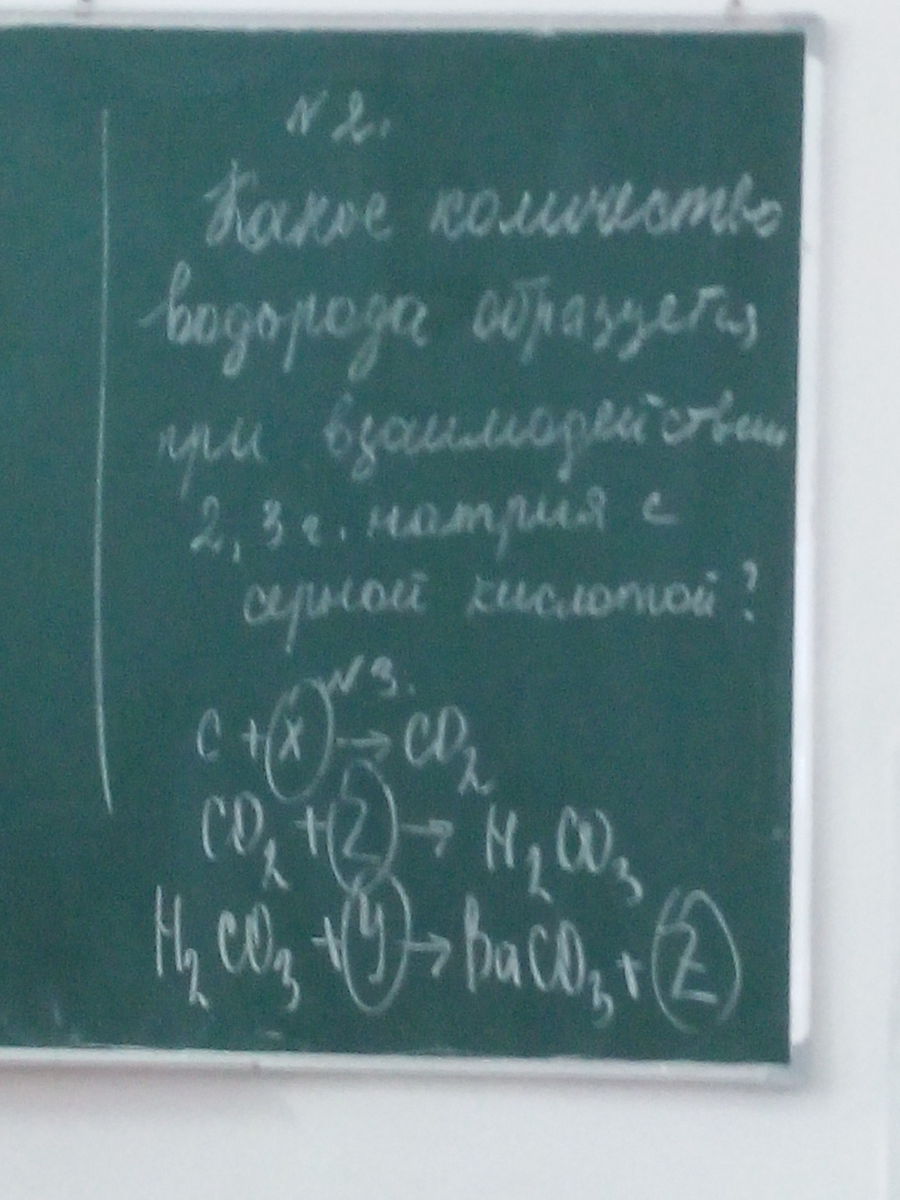
Ответы
Автор ответа:
0
2Na + H2SO4 = Na2SO4 + H2
M(Na) = 23 г/моль
n(Na) m/M = 2.3/23 = 0.1 моль
n(H2) = n(Na)/2 = 0.1/2 = 0.05 моль
Задание 3
С + O2 = CO2
CO2 + H2O = H2CO3
H2CO3 + BaCl2 = BaCO3 + 2HCl
M(Na) = 23 г/моль
n(Na) m/M = 2.3/23 = 0.1 моль
n(H2) = n(Na)/2 = 0.1/2 = 0.05 моль
Задание 3
С + O2 = CO2
CO2 + H2O = H2CO3
H2CO3 + BaCl2 = BaCO3 + 2HCl
Похожие вопросы
Предмет: Химия,
автор: hayhay00
Предмет: Математика,
автор: Аноним
Предмет: Физика,
автор: lagger24252425
Предмет: Математика,
автор: Аноним
Предмет: Алгебра,
автор: 12sashaana45